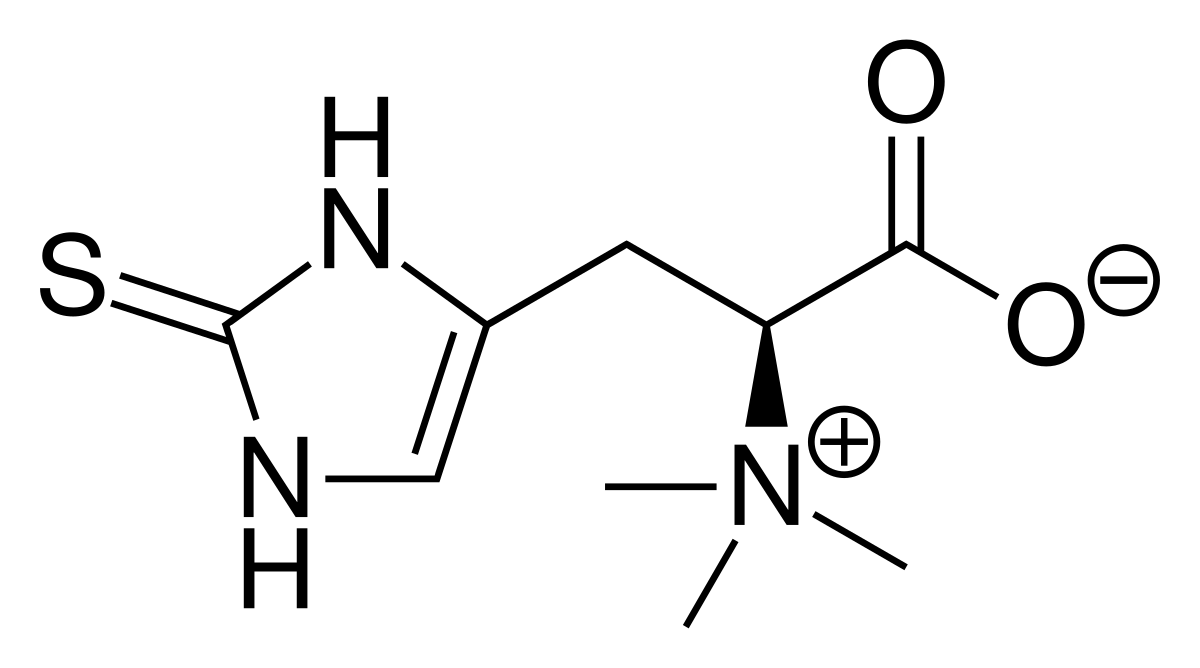
S’ha aprovat la Decisió d’Execució (UE) 2017/1281 de la Comissió de 13 de Juliol de 2017 per la que s’autoritza la comercialització de la L-ergotioneina com a nou ingredient alimentari d’acord al reglament (CE) núm. 258/97 del Parlament Europeu i del Consell.
El 25 de juliol de 2013, l’empresa Tetrahedron va presentar una sol·licitud a les autoritats competents de França per posar al mercat de la Unió la L-ergotioneina sintètica (L-ergotioneina”) com a nou ingredient alimentari a tenor de l’article 1, apartat 2, lletra c), del Reglament (CE) núm. 258/97. La sol·licitud excloïa la utilització per lactants, nens de curta edat i dones embarassades i lactants.
En 2016, la EFSA al seu “Scientific Opinion on the safety of L-ergothioneine as a novel food pursuant to Regulation (EC) No 258/97“, va concloure que la L-ergotioneina era segura per als usos proposats i als nivells indicats.
Les mesures previstes en la present Decisió s’ajusten al dictamen del Comitè Permanent de Vegetals, Animals, Aliments i Pinsos. A més, especifica que podrà comercialitzar-se en la Unió com a nou ingredient per ser utilitzat en complements alimentaris destinats a la població en general, exclosos lactants, nens de curta edat, i dones embarassades i lactants. Així mateix, la denominació de la L-ergotioneina figurarà en l’etiquetat dels productes alimentaris que la continguin.
Pots informar-te sobre la resta de modificacions que introdueix aquest Reglament i sobre com pots estar actualitzat/da de tota la legislació alimentaria al següent enllaç:
http://www.legalimentaria.es
Font: revista alimentaria
